再生医療で人体の再構築ができるのか?の答えを求めて、生体の組織を人工的に再構築する研究分野である組織工学についての論文を綴ります。
わかりやすい紹介を心がけるので少しでもこの分野に興味を持ってもらえると嬉しいです。
今回紹介する論文は「Electrochemical sensing of oxygen metabolism for a three-dimensional cultured model with biomimetic vascular flow」で2022年にBiosensors and Bioelectronics (PubMed)に掲載された論文です。
Organ-on-a-chipという小さなチップの上で臓器を再現しようとする研究の類で、スフェロイドやオルガノイドに血管を通すだけでなく、酸素濃度を測るセンサーを搭載することで、血管が機能的に働いていることをリアルタイムに調べることができた論文です。
「再生医療のアトリエ」は私が大好きな研究である、再生医療・組織工学という人工的に臓器を作る研究について「とにかく楽しく、わかりやすく」をモットーに叡智を綴る場所です。
よかったところ、わかりにくいところ、もっと知りたいところなどコメントいただけると嬉しいです。
研究の背景とか課題とか
再生医療や創薬開発のために、体の外の環境でも(in vitro)生体に似た機能を持った3次元の立体的な構造の組織を作る研究が進められています。
3次元的な構造を作ることの解決すべき課題の一つとして、「厚み」が挙げられます。
これまでの通常の細胞培養では、培養皿の表面に細胞が薄く接着した状態(2次元)で培養するため、細胞は均一にまんべんなく培養液から酸素や栄養素を得ることができていました。
これに対して、3次元の厚みを持つ細胞の塊(組織)では、組織の内部の方への酸素や栄養素の供給がうまく行かずに壊死してしまいます。
2次元培養よりも機能が良くなると言われているスフェロイドやオルガノイドといった細胞の3次元培養が開発されてきていても、より大きく臓器の構造に近づくほど内部が壊死してしまうという状況です。
具体的には、酸素や栄養素が供給されるのは表面から100-200μmとごくわずかであると言われています。(参考:PubMed)
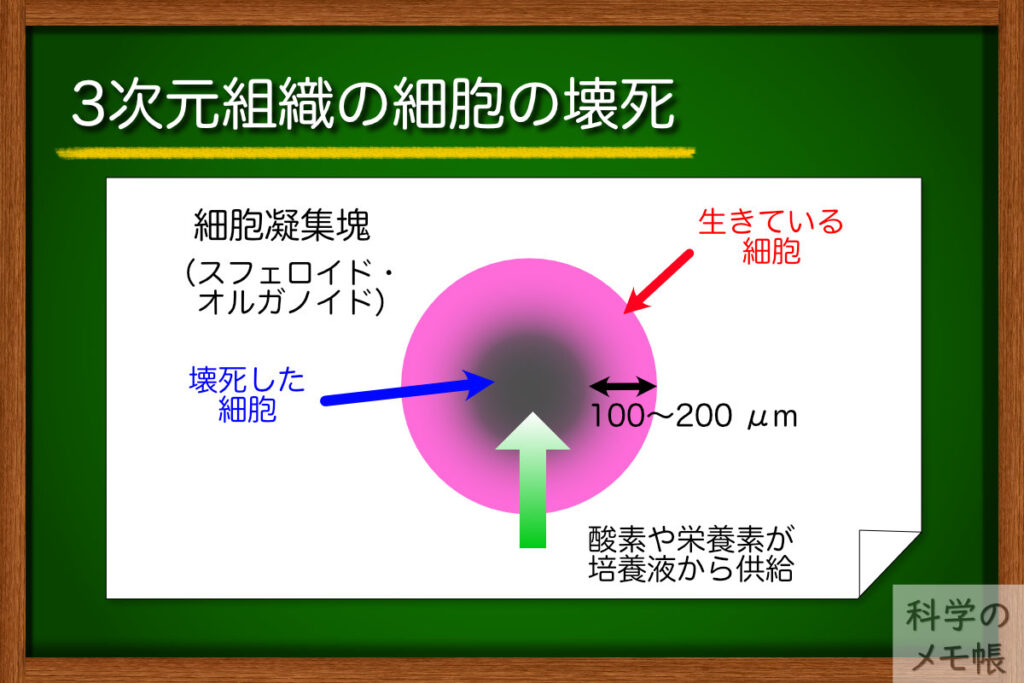
この課題を解決するための方法として考えられているのが、「組織に血管を通すこと」です。
その一例として、積み重ねた細胞シートにたいして、組織に対して培養液を流し込む(灌流する)デバイスを用いて、デバイス側の流路と組織内部の血管をつなげて、組織内部に培養液を届ける個人的におもしろいと感じる技術がありました。(参考:PubMed)
この技術でもまだまだ解決できていない課題はもちろんあり、デバイスの機構としてサイズが大きいため薬剤評価用としては培養のコストが高く量産が厳しいことや、せっかく血管を中に通してもその組織の機能はどれほど高くなったのか?を測定する方法が不足していることが考えられます。
血管デバイスとセンサーを組み合わせて培養と測定をリアルタイムに行う技術
今回ピックアップする論文は、厚みのある組織に血管を通す培養技術を使って組織の高い機能を維持し、同時にその機能を測定できるようなデバイスを構築することに挑戦したものです。
「Electrochemical sensing of oxygen metabolism for a three-dimensional cultured model with biomimetic vascular flow」で2022年にBiosensors and Bioelectronics (PubMed)に掲載された論文です。
Organ-on-a-chipという、小さなチップで臓器を再現しようとする研究分野で、スフェロイドやオルガノイドに血管を通し、同時に酸素濃度を測るセンサーを搭載することで、血管が機能的に働いていることをリアルタイムに調べた結果が報告されていました。
小さなチップ上で培養も測定もできてしまうことから、薬剤評価のスクリーニングなどに応用して培養を始めたら全自動で培養も測定もできてしまう夢のようなデバイスになりそうでワクワクします。
デバイスの特徴としては、流路構造は上段と下段の2層になっており、下段に培養液を灌流することができるような毛細血管構造をもつゲルの土台をつくります。
その土台の上に肺細胞から作られたスフェロイドやがん細胞から作られたオルガノイドを培養することで、土台部分の毛細血管が土台に乗せた3次元組織と連結するというものです。
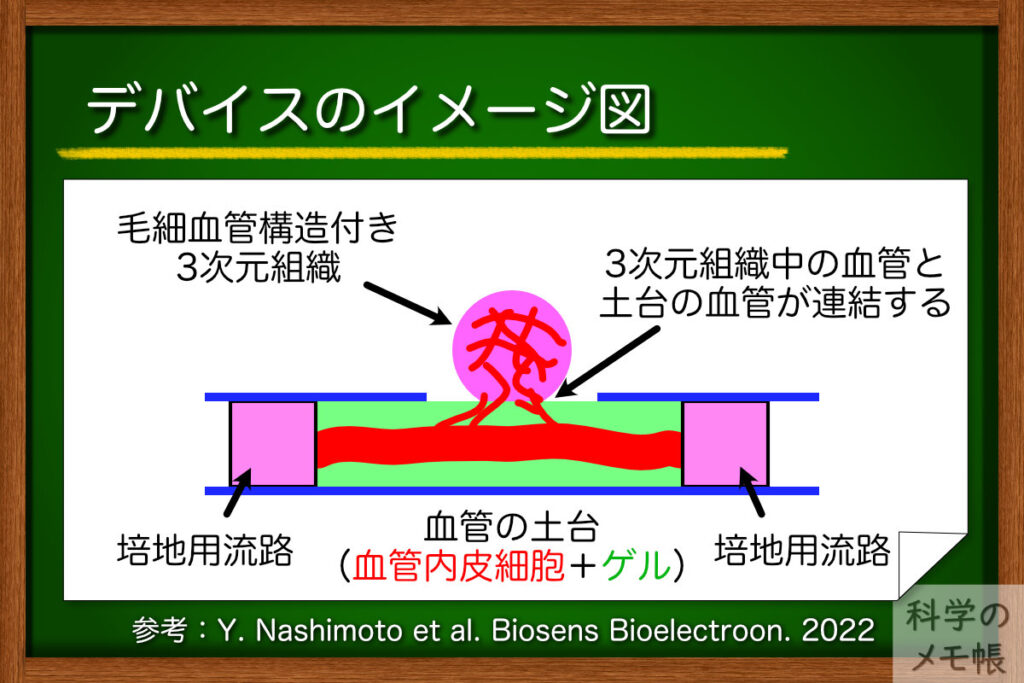
このデバイスで培養した3次元組織は、連結した血管から内部に培養液を流すことができるとのことです。
そして、薬剤を添加した培養液を流し込むことでスフェロイドやオルガノイドの酸素代謝機能が変化していることを、搭載したセンサーでリアルタイムかつ非侵襲的に観察することができたそうです。
従来の研究では形態的な評価によるもので侵襲的であったり時間がかかっていて、リアルタイムかつ非侵襲な評価は難しかったのに対して、
センサーを搭載することでその課題を解決した点が新規性であるとのことです。
血管構造の機能が示されていて面白い
血管構造をもたせた組織構築の研究の論文はこれまで何報か読んできましたが、この論文では血管が薬剤をスフェロイドやオルガノイドの内部へ届ける具体的な機能を示していたことがとても参考になりました。
3次元の細胞を用いて薬剤評価をしたときに、培地に薬を添加するだけでは、組織の外側のみに反応して内側の細胞には効いていないのではないか?というような議論をよくするので、この論文はその議論を深めるために役に立つのかなと感じました。
これまで、Organ-on-a-chipの研究では小さなチップ上でいかに臓器の機能を再現するかということに注力されて来たように感じますが、薬剤のスクリーニングなどに応用しようとするときには、もう一歩進んで機能の評価までを行う必要があります。
自分が読んできたOrgan-on-a-chipの研究の多くは、構造を構築し、顕微鏡や組織学的な手法で評価するため、一つ一つの解析には時間がかかっていて、薬剤のスクリーニングといったたくさんのサンプルを用意して膨大なデータを取得することへの応用が現実的ではなかったように感じます。
今回の論文のように、センサーを用いてリアルタイムかつ非侵襲的に評価することができればそういった課題を解決できるんじゃないかなと期待が高まりました。
血管がつながるまでの栄養供給はどうなる?
気になる点は、スフェロイドとデバイスが血管構造で接続されるまでに5日ぐらい必要なところです。
血管があることでスフェロイド内部に薬剤などを輸送でき、細胞の機能を維持することができるとのことですが、逆に血管がないとそのようなことができないということです。
つまりデバイスと3次元組織の血管構造がつながる前の5日間はスフェロイド内部に酸素や栄養素が十分に供給できていないことが考えられます。
5日間、細胞内部の栄養不足が続くのは、酸素要求度が高い細胞やサイズの大きな3次元組織は壊死する可能性があるのではないか?と思います。
内部壊死しないようなスフェロイドの形成方法の開発や、スフェロイド内部の血管とデバイスの血管の結合をいかに早く行えるかというところを詰める必要がありそうですが、人間の手を加えるには小さすぎる構造なのでなかなかハードルが高そうです。
再生医療とか培養肉でも応用できそう
今回の研究で開発された培養液の灌流機能とセンサー機能を併せ持ったデバイスは、薬剤評価の効率化という点でとても有用な研究であるが、これ以外にも応用の幅は広いのではないかなと感じました。
例えば再生医療では、移植用の組織を作るときは組織の品質を担保する必要があります。
この際に、組織を傷つけずに経時的に観察できる方法が必要とされています。
培養肉の分野では、ウシやトリの筋肉の組織を再現し、培養する方法が考案されています。(参考1:PubMed)(参考2:PubMed)
この分野でも、食べることができるような大きな組織を作るためには血管を使って酸素と栄養素を供給する必要があります。
小さな細胞の塊を食べても「肉!!」って感じはしませんからね。
大きな組織の構築や、培養している間の肉の品質チェックという点でも、このような血管を使った培養デバイスとセンサーを組み合わせた培養方法が有用になってくるのかなと思いました。





コメント